目的
爪白癬患者におけるネイリン®の経口投与開始後の薬物動態、投与開始48週後の有効性及び安全性の検討を行い、本剤の至適用法・用量を評価する。
対象
第Ⅰ趾爪に爪甲混濁部面積比60%以上の病変を有し、直接鏡検で皮膚糸状菌が確認された満20歳以上75歳未満の爪白癬患者94例(100mg連投群:29例、200mgパルス群:31例、400mgパルス群:34例)
方法※
- 100mg連投群 :
- ラブコナゾールとして100mgを1日1回12週間の連続経口投与。
- 200mgパルス群:
- ラブコナゾールとして200mgを1日1回1週間の
経口投与後3週間の休薬を1サイクルとし、3サイクル行う。
- 400mgパルス群:
- ラブコナゾールとして400mgを1日1回1週間の
経口投与後3週間の休薬を1サイクルとし、3サイクル行う。
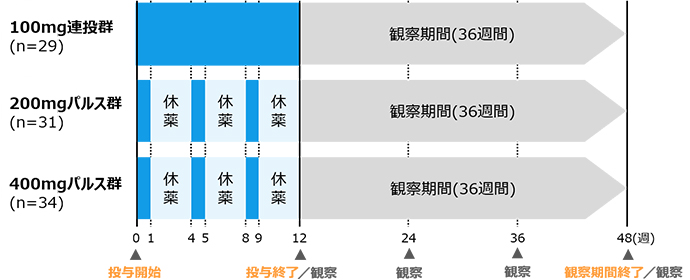
※:試験期間中の総投与量は100mg連投群及び400mgパルス群で8,400mg、200mgパルス群で4,200mgであった。
【用法・用量】 通常、成人には1日1回1カプセル(ラブコナゾールとして100mg)を12週間経口投与する。
評価項目
- 有 効 性 :
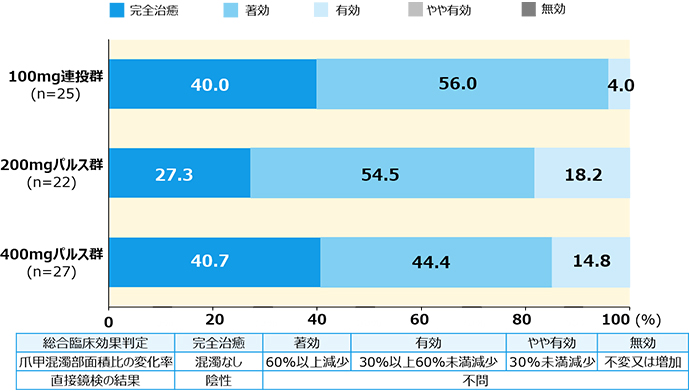
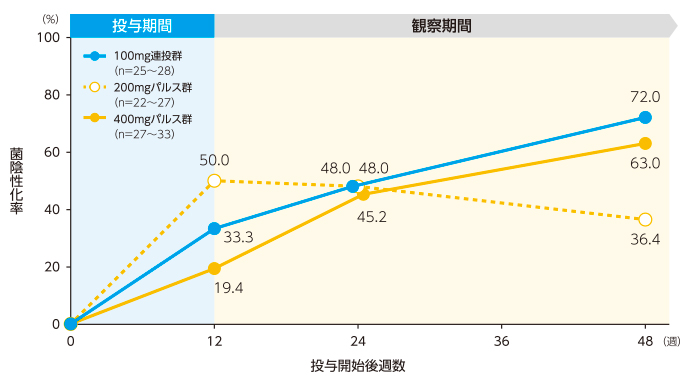
- 投与開始48週後の総合臨床効果、直接鏡検による菌陰性化率 等
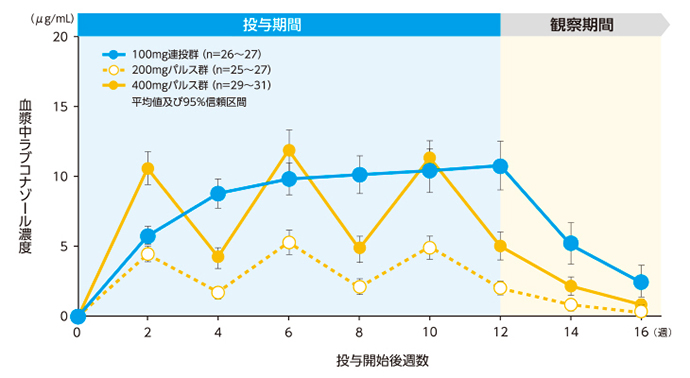
- 薬物動態:
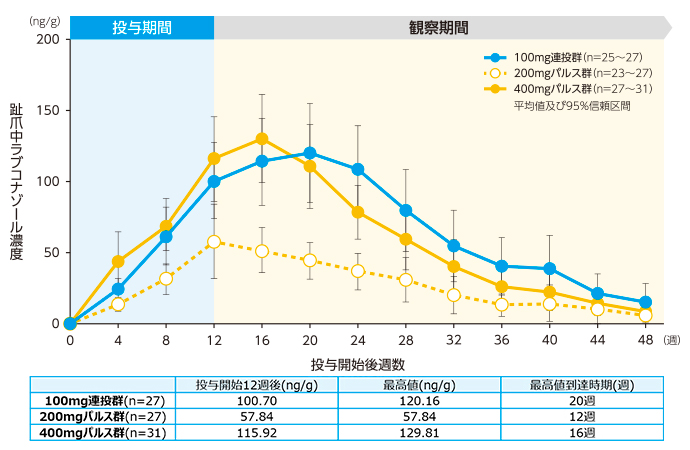
- 血漿中及び爪中ラブコナゾール濃度の推移 等
解析計画
有効性解析対象集団をPPSとし、総合臨床効果は、投与群ごとに完全治癒率、著効率、有効率の頻度集計及び割合を算出した。爪甲混濁部面積比の経時的変化は、測定結果及び投与前値からの変化量について、投与群ごとに各評価時点での記述統計量を算出した。
PPS(Per Protocol Set):治験実施計画書に適合した対象集団